Adenosiinimonofosfaatti "Nukleotidi" on nukleotidi, joka voi edustaa osaa energian kantaja-adenosiinitrifosfaatista (ATP). Syklisenä adenosiinimonofosfaattina se toimii myös toisena sanansaattajana. Se syntyy muun muassa ATP: n hajotessa, mikä vapauttaa energiaa.
Mikä on adenosiinimonofosfaatti?
Adenosiinimonofosfaatti (C10H14N5O7P) on nukleotidi ja kuuluu puriiniribotideihin. Puriini on ihmiskehossa rakennusmateriaali, jota esiintyy myös kaikissa muissa elävissä asioissa. Molekyyli muodostaa kaksoisrenkaan eikä koskaan esiinny yksin: Puriini on aina kytketty muihin molekyyleihin suurempien yksiköiden muodostamiseksi.
Puriini on yksi adeniinin rakennuspalikoista. Tätä emästä löytyy myös deoksiribonukleiinihaposta (DNA) ja se koodaa geneettisesti tallennettua tietoa. Adeniinin lisäksi guaniini kuuluu myös puriiniemäksiin. Adenosiinimonofosfaatissa oleva adeniini on kytketty kahteen muuhun rakennuspalikkaan: riboosiin ja fosforihappoon. Ribose on sokeri, jolla on molekyylikaava C5H10O5. Biologia kutsuu molekyyliä myös pentoosiksi, koska se koostuu viisijäsenisestä renkaasta. Adenosiinimonofosfaatissa fosforihappo sitoutuu riboosin viidenteen hiiliatomiin. Muita adenosiinimonofosfaatin nimiä ovat adenylaatti ja adenyylihappo.
Toiminto, vaikutukset ja tehtävät
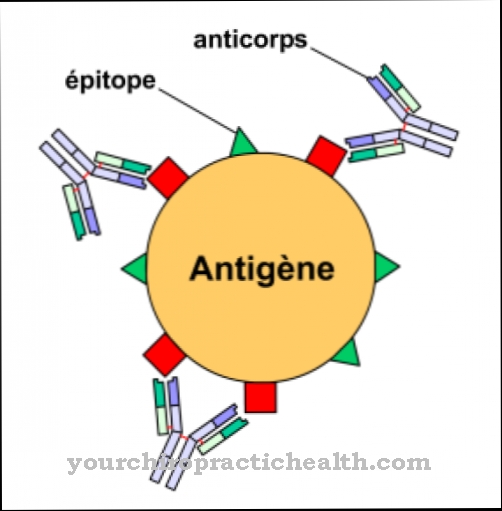
Syklinen adenosiinimonofosfaatti (cAMP) tukee hormonaalisten signaalien siirtoa. Esimerkiksi steroidihormoni sitoutuu reseptoriin, joka sijaitsee solukalvon ulkopuolella. Tietyssä mielessä reseptori on solun ensimmäinen vastaanottaja. Hormoni ja reseptori sopivat yhteen kuten avain ja lukko ja laukaisevat siten biokemiallisen reaktion solussa.
Tässä tapauksessa hormoni on ensimmäinen lähetti, joka aktivoi adenylaattisyklaasin entsyymin. Tämä biokatalyytti jakaa nyt ATP: n soluun, luomalla cAMP. Sitten cAMP aktivoi toisen entsyymin, joka solutyypistä riippuen laukaisee soluvasteen - esimerkiksi uuden hormonin tuotannon. Adenosiinimonofosfaatilla on toinen signaaliaineesi tai toinen lähettiläs.
Molekyylien lukumäärä ei kuitenkaan pysy samana vaiheesta toiseen: Molekyylien lukumäärä kasvaa suunnilleen kymmenkertaiseksi reaktiovaihetta kohti, mikä lisää solun vastetta. Tämä on myös syy siihen, miksi hormonit ovat riittäviä erittäin pieninä pitoisuuksina voimakkaan reaktion käynnistämiseksi. Reaktion lopussa kaikki cAMP: n jäännös on adenosiinimonofosfaattia, jonka muut entsyymit voivat palata sykliin.
Kun entsyymi halkaisee AMP: n adenosiinitrifosfaatista (ATP), syntyy energiaa. Ihmiskeho käyttää tätä energiaa eri tavoin. ATP on tärkein energian kantaja elusolennoissa ja varmistaa, että biokemialliset prosessit voivat tapahtua mikrotasolla samoin kuin lihaksen liikkeet.
Adenosiinimonofosfaatti on myös yksi ribonukleiinihapon (RNA) rakennuspalikoista. Ihmisen solujen ytimessä geneettinen tieto tallennetaan DNA: n muodossa. Jotta solu voi toimia sen kanssa, se kopioi DNA: n ja luo RNA: n. DNA ja RNA sisältävät saman tiedon samasta osasta, mutta eroavat molekyyliensä rakenteessa.
Koulutus, esiintyminen, ominaisuudet ja optimaaliset arvot
Adenosiinimonofosfaatti voi syntyä adenosiinitrifosfaatista (ATP). Adenylaattisyklaasientsyymi halkaisee ATP: n ja vapauttaa energiaa prosessissa. Aineiden fosforihapolla on erityisen tärkeä rooli. Fosforihydridi-sidokset yhdistävät yksittäiset molekyylit toisiinsa. Pilkkomalla voi olla useita mahdollisia tuloksia: joko entsyymit jakaa ATP: n adenosiinidifosfaatiksi (ADP) ja ortofosfaatiksi tai AMP: ksi ja pyrofosfaatiksi. Koska energian metabolia on olennaisesti syklin tapaista, entsyymit voivat myös yhdistää yksittäiset rakennuspalikat takaisin ATP: ksi.
Mitokondriat vastaavat ATP: n synteesistä. Mitokondriat ovat soluorganelleja, jotka toimivat solujen voimalaitoksina. Ne erotetaan muusta solusta omalla kalvollaan. Mitokondriat perivät äidiltä (äiti). Adenosiinimonofosfaattia esiintyy kaikissa soluissa, ja siksi sitä voi löytää kaikkialla ihmiskehossa.
Sairaudet ja häiriöt
Adenosiinimonofosfaatissa voi esiintyä useita ongelmia. Esimerkiksi ATP: n synteesi mitokondrioissa voi olla häiriintynyt. Lääketiede kutsuu myös tällaista toimintahäiriötä mitokondrioksi. Sillä voi olla monia syitä, mukaan lukien stressi, huono ruokavalio, myrkytys, vapaiden radikaalien vahingot, krooninen tulehdus, infektio ja suolistosairaus.
Geneettiset viat ovat usein vastuussa oireyhtymän kehityksestä. Mutaatiot muuttavat geneettistä koodia ja johtavat erilaisiin häiriöihin energian aineenvaihdunnassa tai molekyylien rakenteessa. Näitä mutaatioita ei välttämättä löydy solun ytimen DNA: sta; Mitokondrioilla on oma geneettinen koostumuksensa, joka esiintyy riippumatta solun ytimen DNA: sta.
Mitokondriopatiassa mitokondriat tuottavat ATP: tä vain hitaammin; siksi soluilla on vähemmän energiaa. Sen sijaan, että rakentaisi täydellistä ATP: tä, mitokondrit syntetisoivat enemmän ADP: tä kuin normaalisti. Solut voivat käyttää ADP: tä myös energian tuotantoon, mutta ADP emittoi vähemmän energiaa kuin ATP. Mitokondriaalisessa sairaudessa kehon voi käyttää glukoosia energian toimittajana; kun ne hajoavat, syntyy maitohappoa. Mitokondriaalitauti ei ole itsessään sairaus, vaan oireyhtymä, joka voi olla osa sairautta.
Lääketiede tiivistää mitokondriohäiriöiden erilaiset ilmenemismuodot nimellä. Se voi esiintyä esimerkiksi MELAS-oireyhtymän yhteydessä. Tämä on neurologinen sairaus, jolle on ominaista kouristukset, aivovauriot ja lisääntynyt maitohapon muodostuminen. Lisäksi mitokondriaalinen sairaus liittyy myös dementian eri muotoihin.

.jpg)



.jpg)